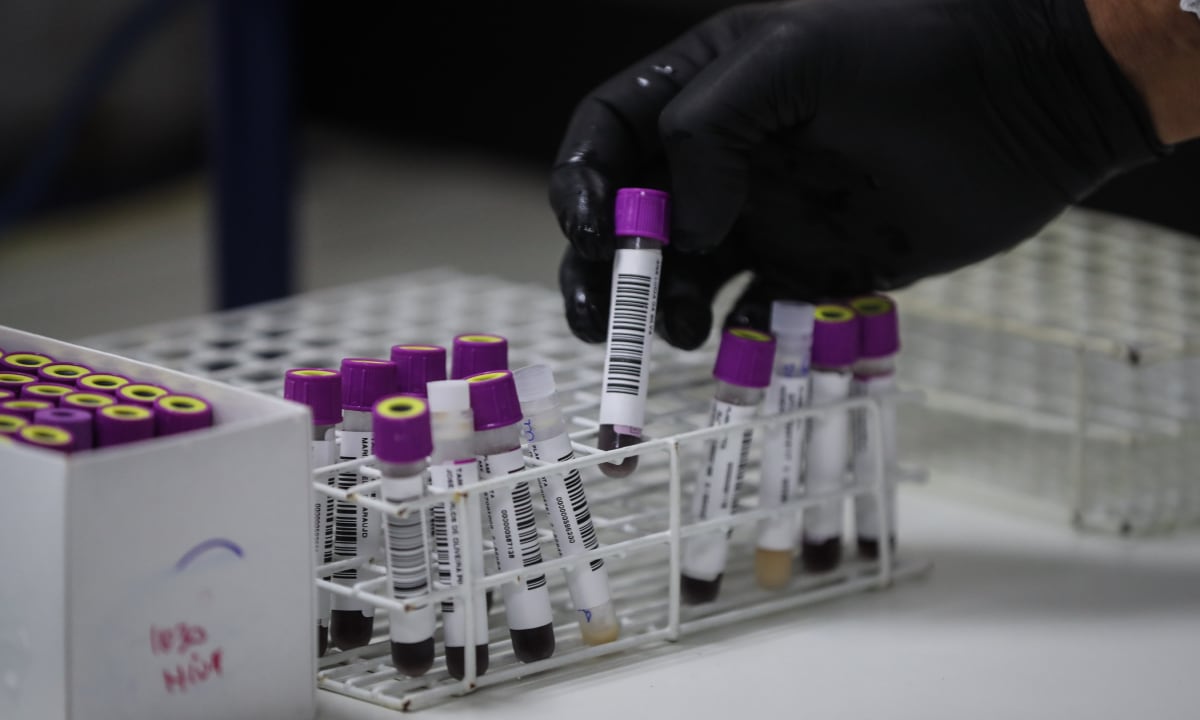
El Perú se ha sumado a los esfuerzos internacionales para el desarrollo de una vacuna contra el virus de inmunodeficiencia humana (VIH). En la Universidad Nacional Mayor de San Marcos (UNMSM), un equipo de investigadores realiza ensayos clínicos y estudios de tratamientos preventivos, como parte de una red científica global.
Estas investigaciones se desarrollan en el Centro de Investigaciones Tecnológicas, Biomédicas y Medioambientales (CITBM), a través de su Unidad de Ensayos Clínicos (UNIDEC), responsable de la gestión de estudios clínicos e investigación biomédica en el país.
Ensayos clínicos en coordinación internacional
Uno de los ensayos actualmente en curso está enfocado en la vacuna contra el VIH. El CITBM cumple la función de laboratorio de referencia para una red mundial de investigación coordinada por la División de VIH del Instituto Nacional de Alergias y Enfermedades Infecciosas de Estados Unidos (NIAID).
Además del VIH, el centro ha participado en investigaciones relacionadas con covid-19, viruela del mono, zika, tuberculosis y hepatitis C, consolidando su rol en el estudio de enfermedades infecciosas.
En UNIDEC se realizan pruebas de detección y confirmación del VIH, que incluyen test rápidos, moleculares y de carga viral, fundamentales para evaluar a los participantes de los estudios clínicos.
Rigor científico y seguridad de los estudios
En entrevista con la Agencia Andina, la doctora Leonela Candia, médico patólogo de UNIDEC, explicó que los ensayos siguen un proceso estricto desde la toma de muestras hasta su envío a Estados Unidos para análisis especializados.
“Estos ensayos clínicos buscan primero determinar que la vacuna sea segura para poder distribuirla a nivel mundial y, además, que sea efectiva para evitar nuevos contagios por VIH”, precisó.
La especialista destacó que el CITBM cuenta con uno de los pocos laboratorios del país certificados para aislar células polimorfonucleares, fundamentales para evaluar la respuesta inmunológica generada por las vacunas.
“Estas células permiten determinar si la respuesta inmunológica ha sido adecuada. Las aislamos y las enviamos congeladas a Estados Unidos para su evaluación”, detalló.
Proceso de evaluación de los participantes
El laboratorio de UNIDEC aplica un protocolo estandarizado de alta calidad, que inicia con un tamizaje o screening para verificar que los voluntarios cumplan con los criterios del estudio.
Todos los participantes brindan su consentimiento informado, y se les realizan diversas pruebas para determinar su estatus de VIH, entre ellas:
- Pruebas rápidas
- Pruebas de antígenos y anticuerpos
- Pruebas confirmatorias (Genius)
- Pruebas moleculares (Ginexper)
- Pruebas de carga viral
Posteriormente, las muestras se separan en plasma, suero y células polimorfonucleares, que son empaquetadas, congeladas y conservadas hasta su envío.
Ensayo Mosaico y cooperación regional
UNIDEC también participa en el ensayo denominado “Mosaico”, orientado a medir la eficacia de la vacuna en poblaciones con mayor riesgo de contraer el VIH. Además, funciona como laboratorio de referencia para centros de investigación de México y Argentina, procesando muestras provenientes de dichos países.
Un software especializado permite asegurar la trazabilidad completa de cada muestra, desde su recolección hasta su procesamiento final. Los datos son analizados estadísticamente en Estados Unidos para determinar la efectividad clínica de la vacuna.
Avances, desafíos y nuevos ensayos
La doctora Candia recordó que en 2017 se desarrolló un ensayo clínico de gran envergadura que no alcanzó los resultados esperados tras cinco años de investigación. Sin embargo, el estudio permitió identificar que la molécula de la vacuna generaba respuesta inmunológica en células CD4 y CD8, aunque no suficiente.
Ese hallazgo dio origen a nuevos ensayos clínicos, entre ellos el HBTN206, del cual el Perú forma parte actualmente.
Los ensayos clínicos pueden extenderse entre dos años en fases de seguridad y hasta cinco o seis años en fases de eficacia, con evaluaciones anuales de los datos. Según la especialista, el éxito de estos estudios depende no solo de la respuesta inmunológica, sino también de factores sociodemográficos y conductuales de los participantes.